上海百趣生物科技有限公司
13 年
手机商铺
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 2.7
- 2.7
推荐产品
公司新闻/正文
秒懂百科 | 3分钟带您了解蛋白泛素化修饰
4476 人阅读发布时间:2022-06-13 15:29
人体细胞内蛋白质降解主要有两条途径:
一种是在溶酶体内(一种具有“消化降解”功能的细胞器)通过ATP(体内直接供能分子)非依赖途径被降解,此途径主要降解外来的蛋白质,对蛋白质的选择性较差。
另一种是在蛋白酶体内,通过ATP依赖途径(需耗能),经过泛素化修饰后被降解。此途径主要降解细胞内结构异常的蛋白质和短寿的蛋白质。
如果我告诉你真核生物80%~90%蛋白质的降解是由泛素-蛋白酶体降解途径(ubiquitin-pro-teasomepathway, UPP)介导的,而此途径是泛素化修饰蛋白最主要的去向,你是不是很好奇泛素化修饰到底是何方神圣?
那小编就言简意赅、简明扼要的给大家介绍一下蛋白泛素化修饰。
泛素化修饰概念
泛素(Ub, ubiquitin)是一种普遍存在于真核细胞中的由76氨基酸残基组成的多肽。一个或多个泛素分子能够在一系列酶的作用下共价连接至蛋白质底物上,形成泛素化修饰(ubiquitination)。调控蛋白表达水平的重要机制,参与了几乎所有生命过程,是一种至关重要的翻译后修饰。
泛素化修饰过程
01.在ATP供给能量的情况下,泛素激活酶E1将泛素分子活化。
02.泛素激活酶E1将活化的泛素分子传递给泛素结合酶E2。
03.泛素连接酶E3将结合E2的泛素连接到靶蛋白上。

图1. 泛素化修饰过程[1]
泛素-蛋白酶体途径(UPP)
20S催化核心与19S调节复合物结合形成26S蛋白酶体结构。泛素标记的蛋白质与19S复合物结合,并在蛋白水解β亚基处降解。19S亚单位与多泛素链结合,ATP展开蛋白质底物并将其转移到20S核心颗粒中。蛋白质通过20S中心,在那里被降解成25个氨基酸以下的小寡肽。介导泛素非依赖性蛋白质降解。
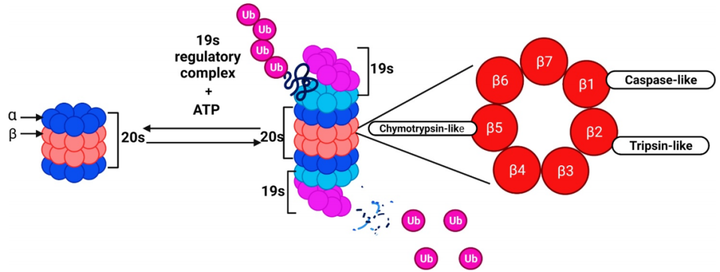
图2. 蛋白酶体结构与蛋白质降解[1]
泛素化修饰类型
在泛素链中,泛素部分可通过其赖氨酸(Lys11、Lys27、Lys6、Lys29、Lys33、Lys63和Lys48)或N端蛋氨酸残基(Met1)结合。每条链由不同的泛素结合域识别,靶向特定信号通路中的蛋白质。Lys48-和Lys63连接链是最丰富的两种链类型,分别调节蛋白酶体降解和各种蛋白水解和非蛋白水解过程。
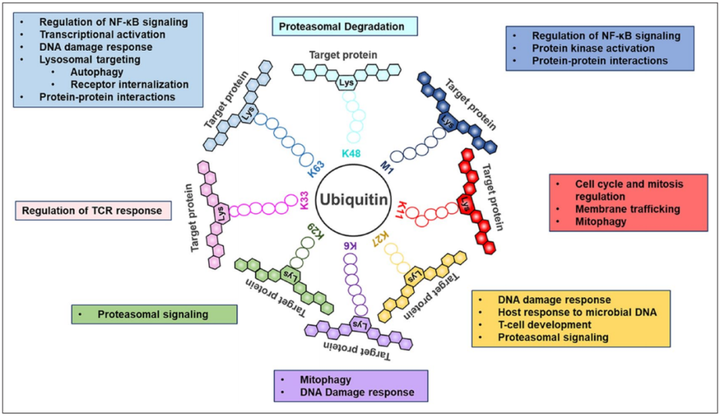
图3. 泛素化修饰类型及其相关生物学作用[2]
泛素化修饰研究方法
质谱是研究泛素化修饰的主要平台,超过95%的PTM的当前数据来自基于MS的蛋白质组研究。泛素化修饰蛋白组学研究方法用于识别其主要目标中的UB修饰位点,并结合特定蛋白质或特定细胞器中UB链连接类型进行定量分析。从不同条件下纯化的蛋白质通过亲和纯化或抗体进行UB修饰肽段的富集。数据分析可以解释研究对象如何响应不同的扰动而改变修饰水平。
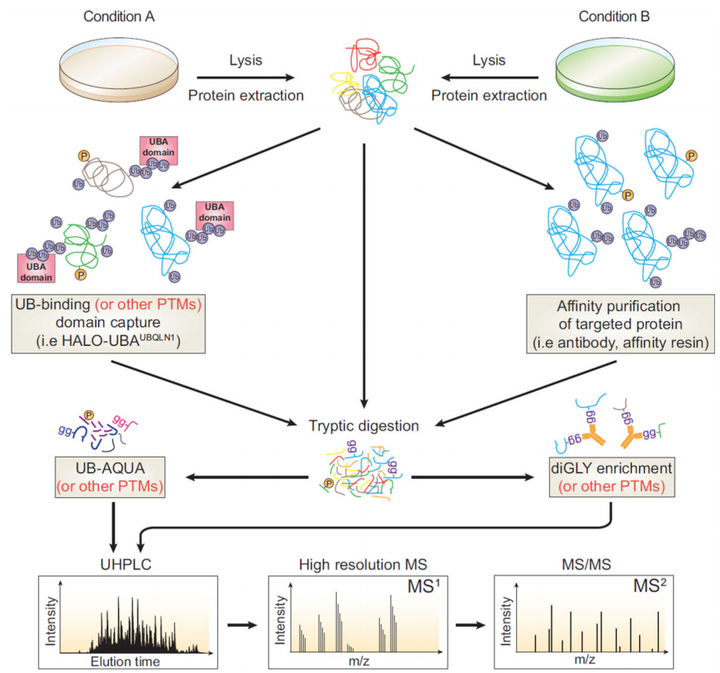
图4. 泛素化修饰蛋白组学研究方法[3]
泛素化修饰定位方法
A.蛋白质进行胰蛋白酶消化后,根据泛素化底物上的Lys-ε-Gly-Gly的基序进行单克隆抗体的免疫沉淀。通过LC-MS/MS对样品进行进一步处理和分析。
B.泛素抗体识别泛素的最后13个氨基酸。富集的泛素化蛋白质由MS进一步分析。此方法不能用于研究线性泛素化。
C.Ub-COFRADIC方法区分游离(α或ε)伯胺和修饰伯胺,以便识别泛素化Lys残基。胰蛋白酶裂解Arg残基的C端。在第一次反相(RP)-HPLC运行后收集的肽处理,进行RP-HPLC和MS。
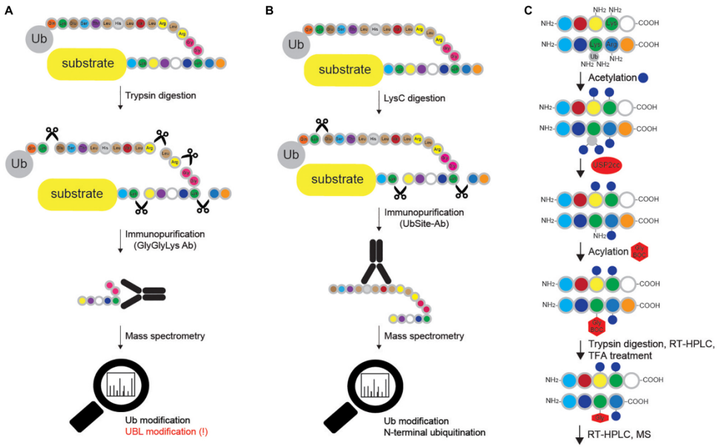
图5. 蛋白质泛素化位点的定位方法[4]
泛素化修饰蛋白组案例赏析
ef="https://book.yunzhan365.com/jtuc/hhxb/mobile/index.html">文章标题:USP14底物的蛋白质组分析揭示了其通过稳定FASN在肝脂肪变性中的作用
PMID:30425250 Nat Commun 20181113;9(1)
泛素特异性蛋白酶14(USP14)是一种主要的蛋白酶体相关的去泛素化酶,对蛋白质组内环境稳定至关重要。作者对USP14底物筛选进行了蛋白质组、泛素化修饰蛋白组和相互作用分析。生物信息学分析揭示了USP14广泛的新潜在作用,尤其是在脂质和碳水化合物代谢过程。发现USP14的过度表达促进了小鼠肝脏甘油三酯的积累,而USP14的基因消融或药物抑制改善了肥胖小鼠的肝脂肪变性、高血糖和胰岛素抵抗。此发现首次揭示了USP14稳定脂肪酸合成酶在肝脂肪变性中不可或缺的作用。
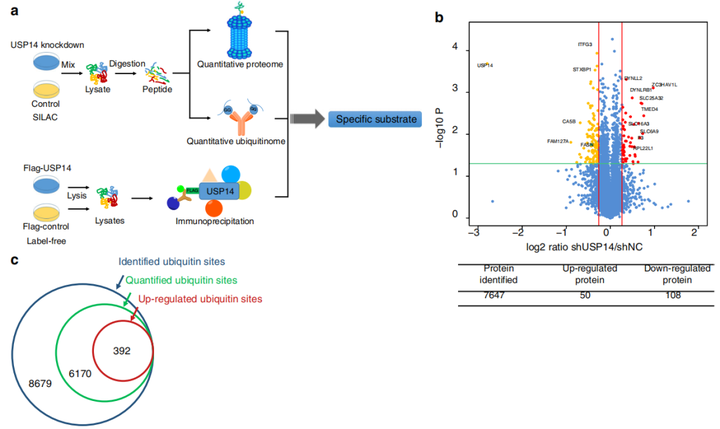
图6. 泛素化修饰蛋白质组学与蛋白互作分析[5]






