上海百趣生物科技有限公司
13 年
手机商铺
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 2.7
- 2.7
推荐产品
公司新闻/正文
Eur. Heart J. IF=39.3! 突破性进展!代谢流揭示白血病化疗心脏毒性新机制!
950 人阅读发布时间:2024-06-14 09:17

文章标题:Rescue of cardiac dysfunction during chemotherapy in acute myeloid leukaemia by blocking IL-1α
发表期刊:European Heart Journal
合作单位:上海交通大学医学院附属儿童医学中心
影响因子:39.3
百趣提供服务:代谢流
研究背景
2024年4月12日,上海交通大学医学院附属儿童医学中心张浩/刘一为老师团队在European Heart Journal杂志上发表了题为Rescue of cardiac dysfunction during chemotherapy in acute myeloid leukaemia by blocking IL-1α的文章。该研究对AML患者的心脏组织和给予DNR治疗的AML小鼠模型进行心脏能量代谢和心功能的变化评估,在百趣生物提供的代谢流服务的基础上探究了心脏能量代谢中脂肪酸代谢和心肌葡萄糖代谢机制。本研究还发现肿瘤来源的白细胞介素1(IL-1α)破坏了心脏代谢,导致DNR治疗后心功能受损。最后,该研究提出IL-1α治疗法可能是减轻AML患者化疗后产生的心脏毒性的一个很有前途的治疗靶点。
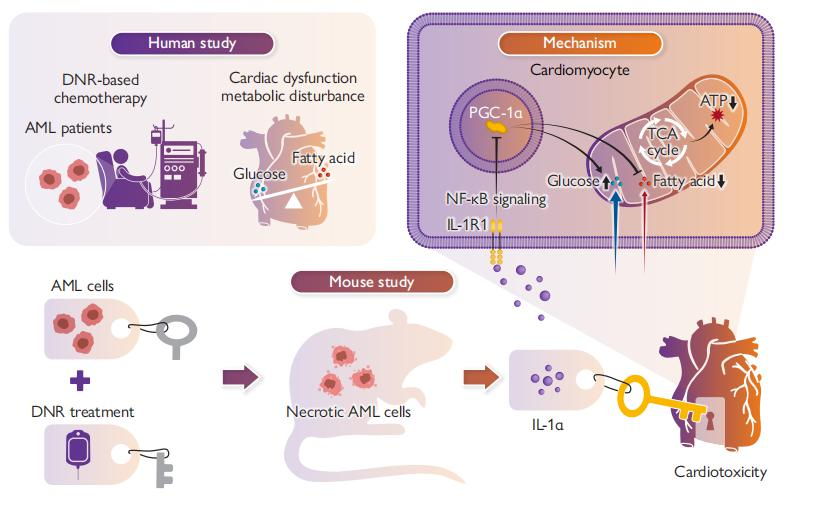
图形摘要:阻断IL-1α挽救AML患者化疗期间的心功能不全的研究
研究结果
1. DNR治疗后AML患者的心肌细胞代谢变化
为了探讨化疗后相关心功能障碍的机制,该研究收集了一名DNR化疗后发生心力衰竭的AML患者和一名年龄匹配的心功能正常并诊断为脑死亡的患者,对其心脏组织进行了心功能分析(图1A-C),在单细胞RNA测序技术上将起源细胞分为8种细胞类型(图1D)。通过对差异表达基因(differentially expressed genes, DEGs)的通路富集分析发现来自AML患者的心肌细胞的代谢过程明显受到干扰(图1E)。
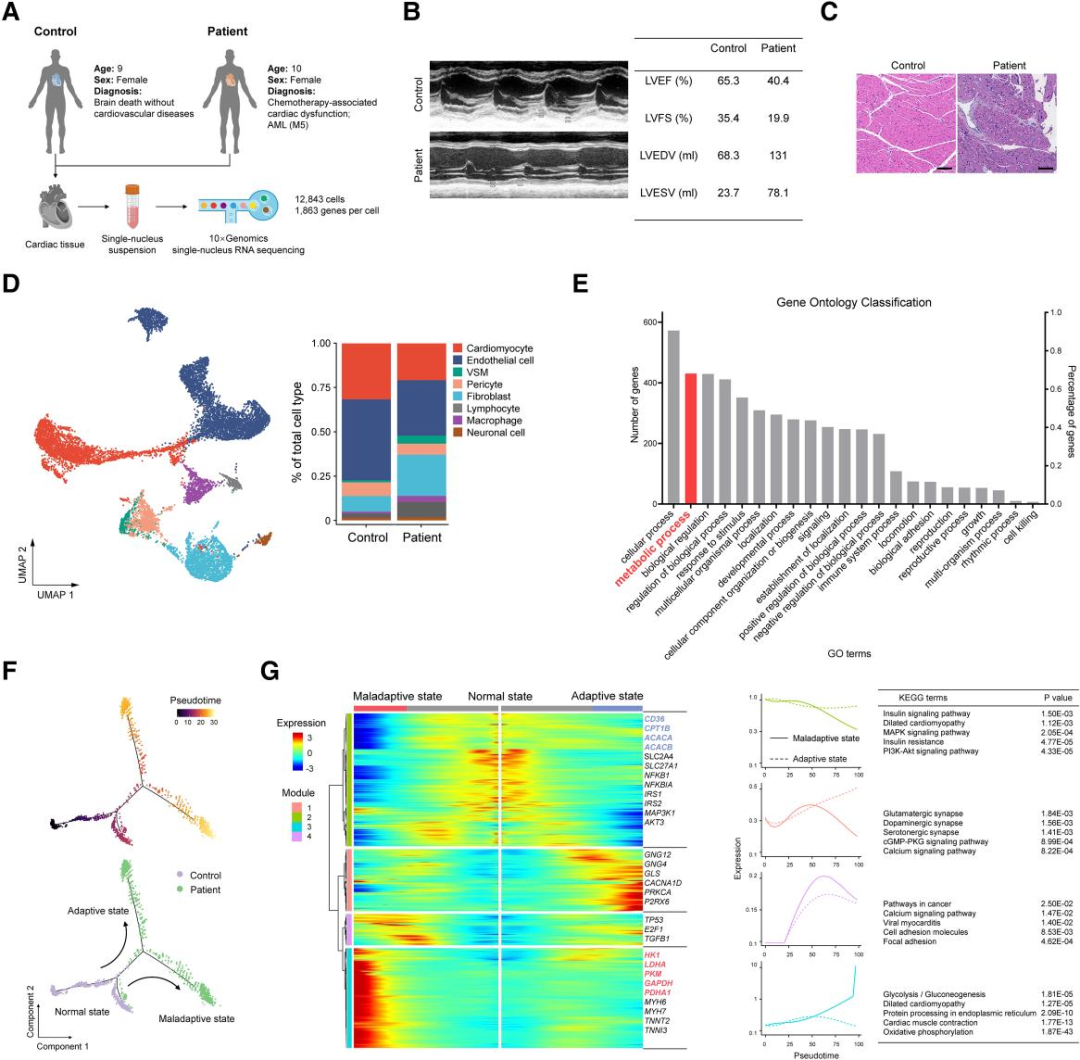
图1. AML患者经DNR型化疗后心肌细胞代谢中
随后在伪时间内对两个样本的心肌细胞进行独特分布(图1F),与适应状态相比,心肌损伤相关基因表达显著增加,脂肪酸代谢相关基因显著下调,糖酵解相关基因显著上调(图1G)。综上分析,该研究发现部分心肌细胞在DNR型化疗后出现代谢紊乱,这种不良适应的代谢状态表现为心肌损伤和心功能不全的。
2. 构建AML小鼠模型探索DNR治疗后心肌损伤和心功能障碍
为了研究DNR化疗对AML患者的心脏代谢和功能影响,该研究设计将MLL-AF9 AML小鼠随机分为两组,建立了用DNR治疗的AML小鼠模型(AML+DNR小鼠)(图2A和B),发现AML+DNR小鼠的脂肪酸摄取显著降低,心肌葡萄糖摄取显著增加(图2C),这些代谢变化与AML+DNR小鼠的心脏ATP水平降低相关(图2D),其表现为破裂的肌纤维之间的线粒体排列略少,偶尔可见嵴的轻微扩张(图2E)。还发现AML+DNR小鼠的基础呼吸、最大耗氧量、ATP产生率和呼吸潜力显著降低(图2F和G)。
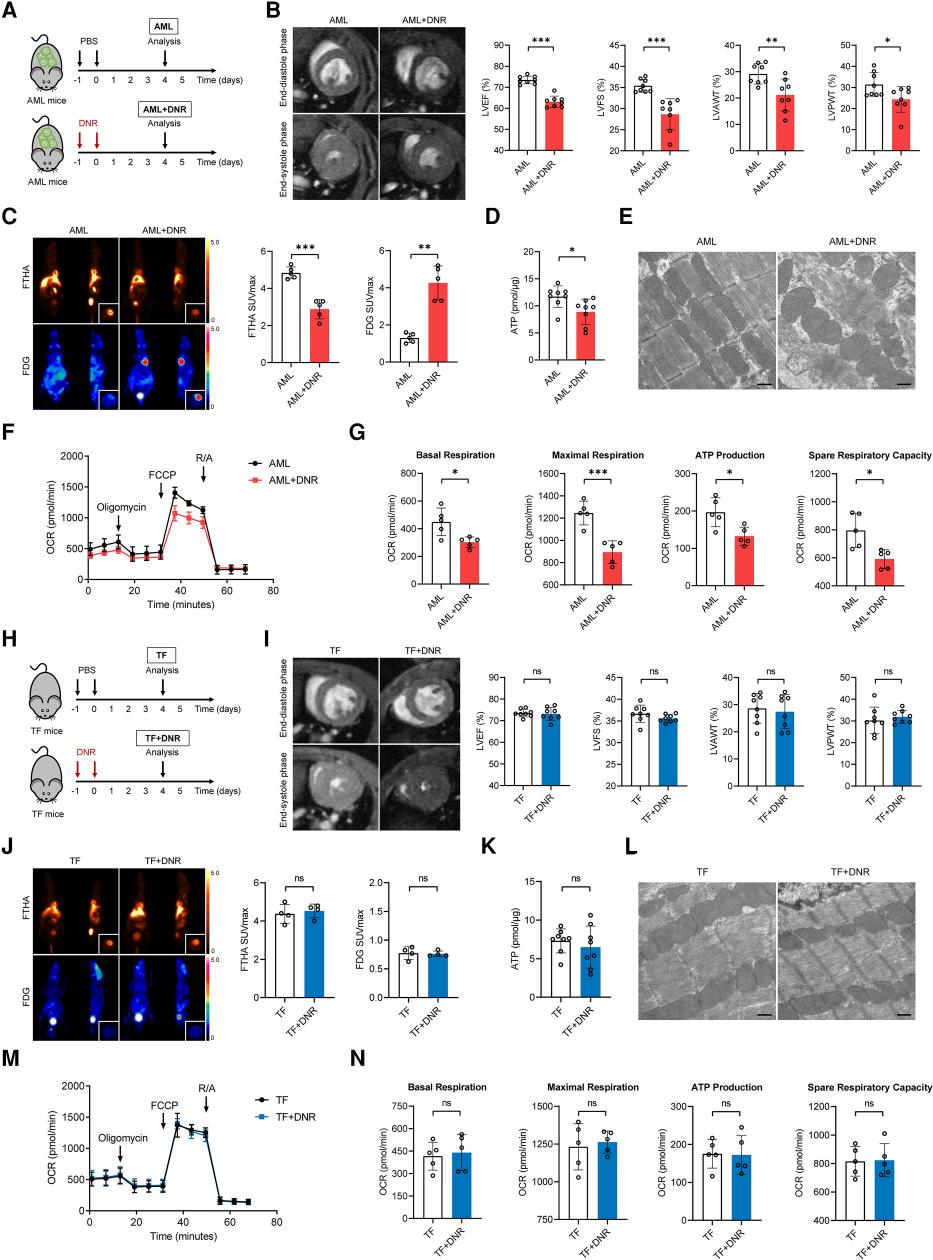
图2. 经DNR治疗后AML小鼠的心脏代谢紊乱和心脏功能受损
那么DNR治疗会不会直接导致心脏代谢功能的重构?研究发现,TF+DNR小鼠的心脏收缩功能,脂肪酸和葡萄糖摄取(图2H-K),线粒体结构和功能(图2L-N)都无显著性变化。因此,研究中使用的DNR剂量对TF小鼠的心脏能量代谢或心功能没有明显影响。在后续实验中使用AML小鼠可以代替TF小鼠来探讨DNR诱导心功能障碍的机制。
3. 同位素标记代谢组学分析AML+DNR小鼠是否诱导心脏底物的重构
从上述结论中推测底物重构可能导致心脏能量缺乏。通过百趣生物提供的同位素标记的代谢流通路示踪分析脂肪酸利用率(图3A-C,[U-13C]棕榈酸通量组分析),发现DNR治疗后AML小鼠使用脂肪酸衍生碳的能量程度低于对照组(图3C和D)。在[U-13C]葡萄糖通量组分析中(图3E和F),AML+DNR小鼠在糖酵解和三羧酸循环(TCA)代谢中13C标记中间体呈现出更大程度的降低(图3G-I),化疗后葡萄糖产生能量的使用增加。在定量分析中发现AML+DNR小鼠中的TCA中间产物水平明显低于AML小鼠(图3J),这表明心脏中葡萄糖分解代谢的增加则不能弥补脂肪酸利用受损而导致的能量生产减少。
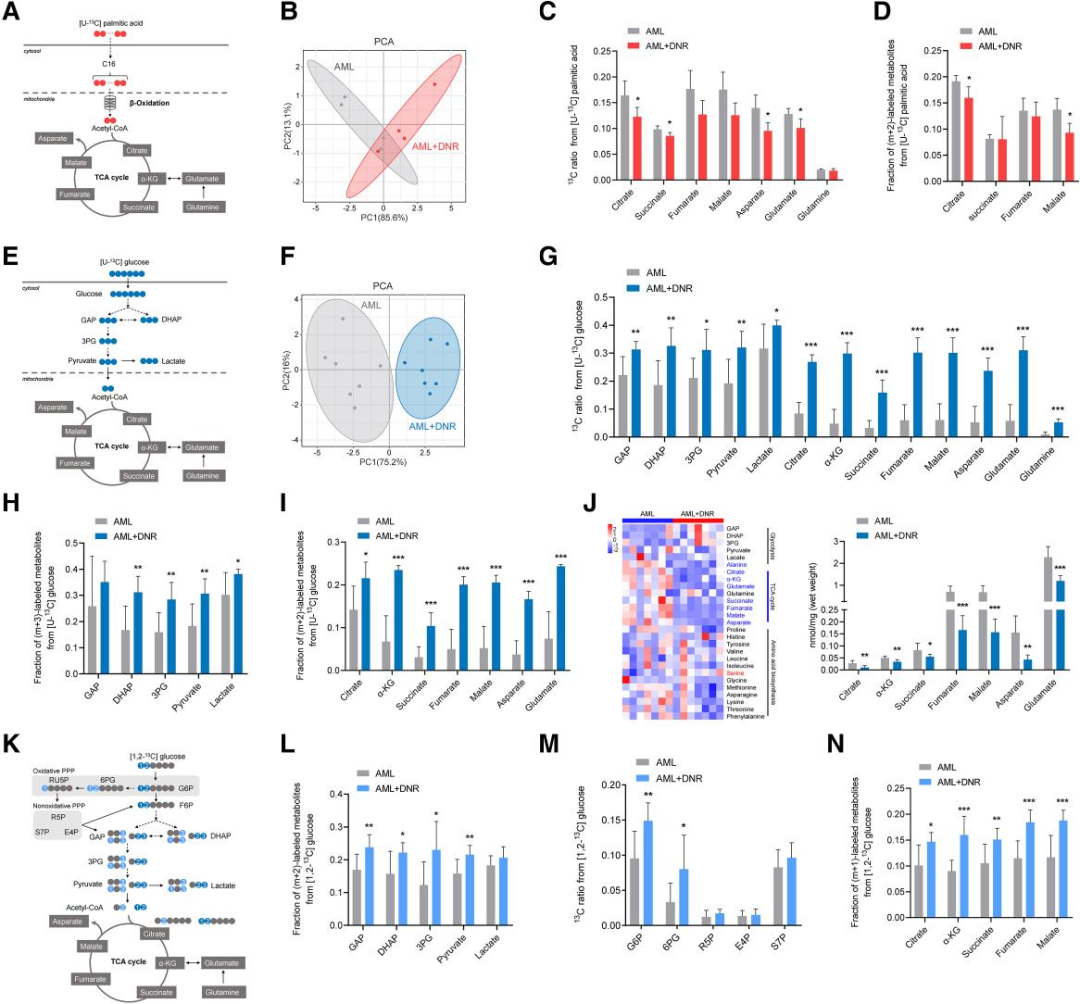
图3. 同位素标记代谢组学通路追分析AML小鼠和AML+DNR小鼠的脂肪酸代谢和葡糖糖代谢
那么心肌葡萄糖代谢的增加否被分流到其他代谢途径中,通过[1,2-13C]葡萄糖通量组分析揭示了糖酵解和其他途径中的葡萄糖通量分布(图3K-L)。13C标记6-磷酸葡萄糖酸和m+1标记的TCA中间体在AML+DNR小鼠组明显大于AML小鼠组(图3M-N),研究证明AML+DNR小鼠心脏中更多的葡萄糖通过磷酸戊糖途径(PPP)进入TCA。综上所述,AML+DNR小鼠会发生干扰心脏脂肪酸代谢,增加葡萄糖利用,来弥补脂肪酸利用的受损的现象。
4. AML+DNR小鼠的心脏能量代谢的干扰原因-IL-1α因子
为了心脏能量代谢紊乱的上游因素,该研究比较了AML和AML+DNR小鼠的心脏中DEGs(图4A和B)。研究发现细胞因子信号通路可能导致AML+DNR小鼠心脏代谢紊乱(图4A)。通过筛选发现存在显著差异的是血浆细胞因子,分析发现IL-1α可能是参与这一现象的关键因素(图4B)。另外,在心肌组织中IL-1α的免疫荧光染色上也显示出相似的趋势(图4C和D)。
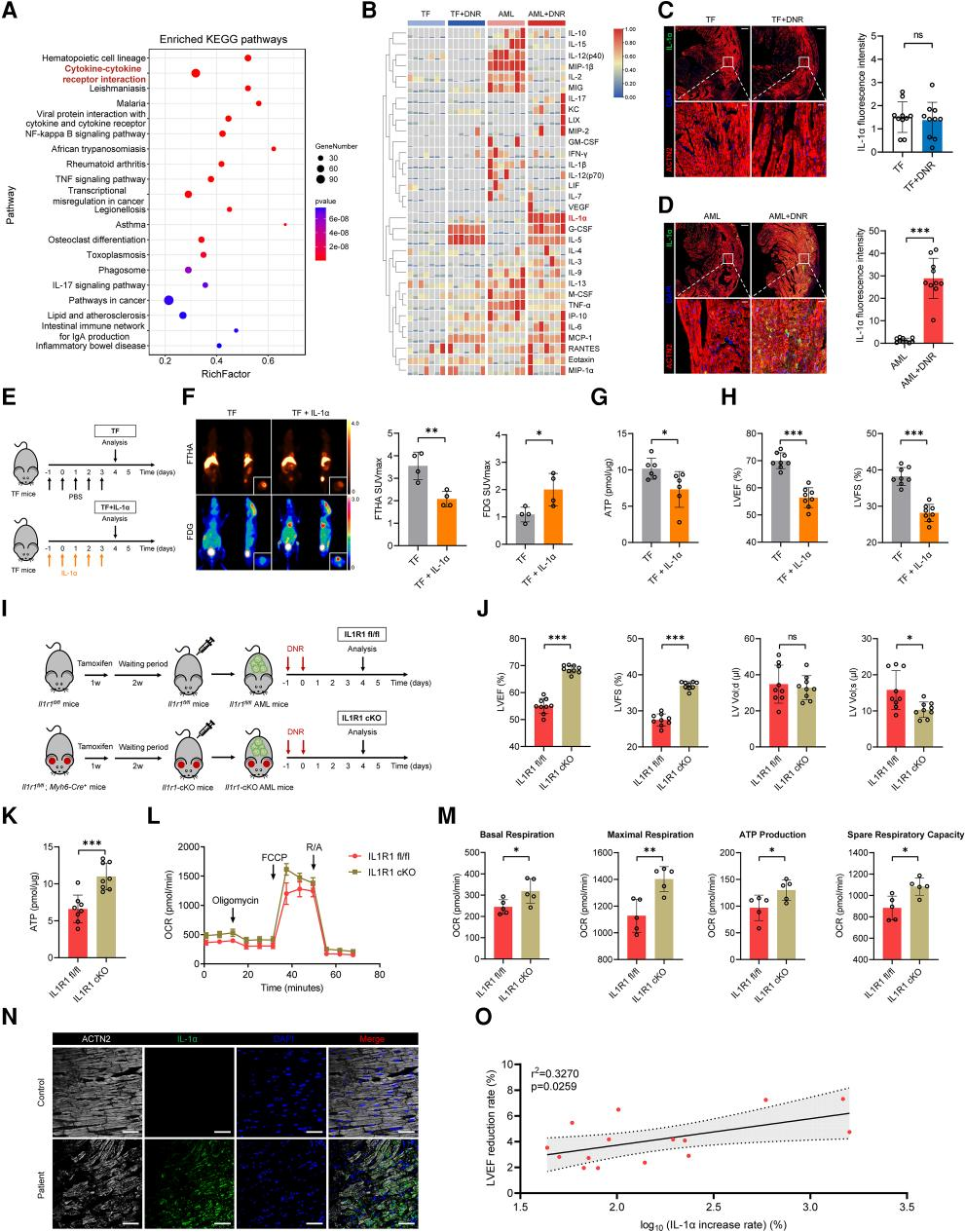
图4. IL-1α因子水平导致了心脏代谢功能的失调
那么IL-1α是否会在体内干扰心脏能量代谢和损害心脏功能?研究发现IL-1α治疗组直接破坏了TF小鼠的心脏代谢和心脏功能(图4E-H)。在带有敲除心肌特异性表达IL1R1的AML小鼠经DNR治疗后发现心脏功能显著改善(图4I-M)。在人体中,AML患者的心脏组织中也发现IL-1α蛋白水平同样升高(图4N)。从另外15名接受DNR治疗的AML患者血浆中发现,IL-1α浓度的增加与左心室射血分数(LVEF)的降低呈正相关(图4O)。综上所述,DNR治疗后AML小鼠血浆IL-1α水平升高,进一步干扰心脏代谢,损害心脏功能。
5. IL-1α因子的主要来源于化疗期间的急性髓系白血病细胞
基于上述结论,研究推测DNR化疗后对肿瘤细胞的损伤可能会诱导肿瘤部位产生大量IL-1α因子。从体外实验显示,随着DNR浓度的增加,坏死细胞的比例显著增加(图5A),THP-1细胞沉淀物和培养上清液中IL-1α蛋白表达水平显著升高(图5B和C)。在AML+DNR小鼠动物实验中发现约20%的肿瘤细胞出现坏死(图5D),小鼠骨髓中坏死肿瘤细胞的数量和IL-1α的荧光强度均增加(图5E和F)。这些结果表明AML+DNR小鼠肿瘤细胞可能释放IL-1α。那么IL-1α主要来自肿瘤细胞还是非肿瘤细胞?研究建立了全面敲除IL-1α(IL-1α−/−, IIL-1α-KO)小鼠模型并注射MLL-AF9 AML细胞(图5G)。结果发现在IL-1α-KO小鼠中,DNR治疗后IL-1α荧光强度和受损的心功能并没有得到缓解(图5H-J)。因此,化疗后血浆中检测到的IL-1α并非主要来自非肿瘤细胞。
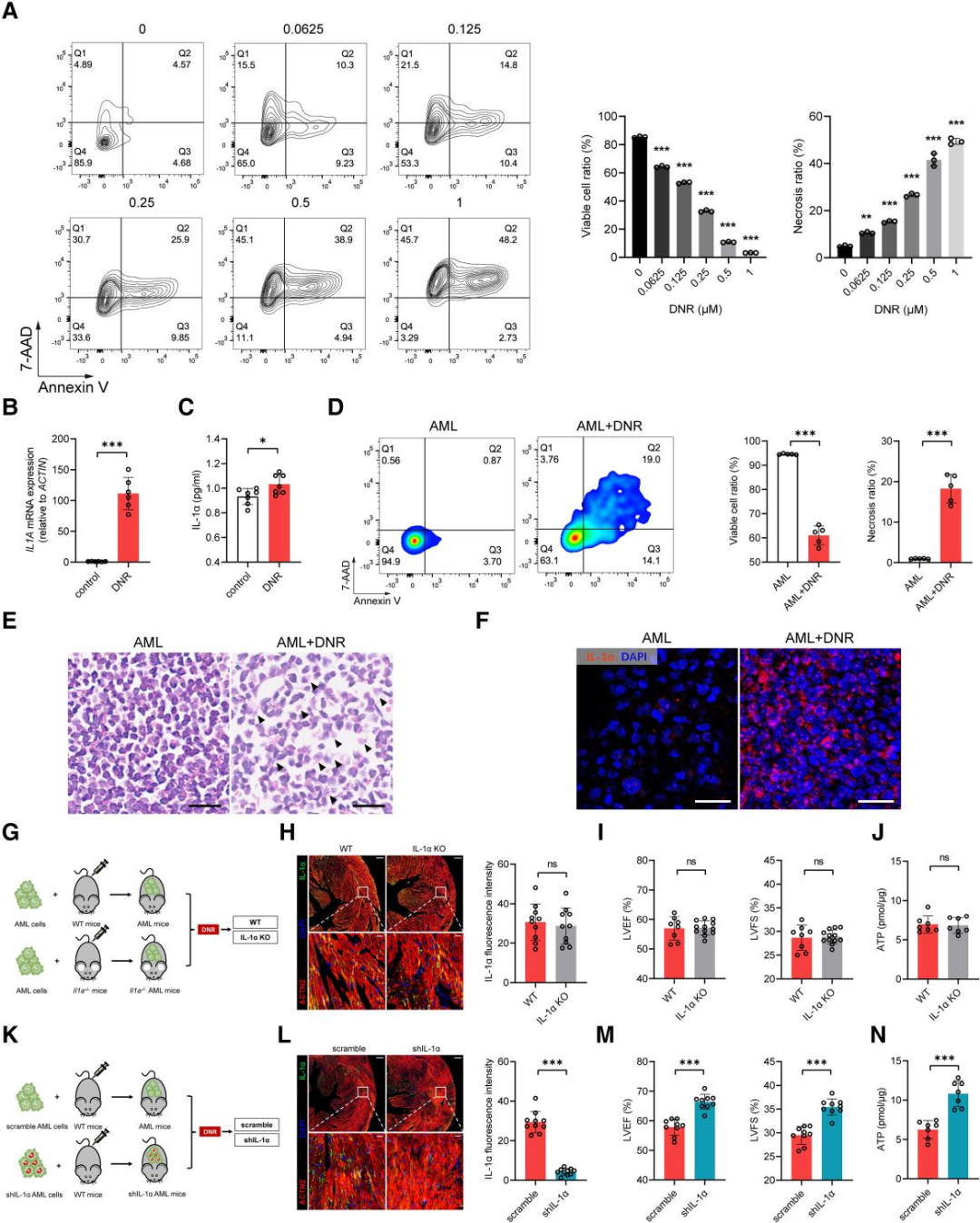
图5. 经DNR治疗后的AML小鼠坏死肿瘤中AML细胞会释放出IL-1α
为了证明IL-1α主要来自肿瘤细胞,研究构建了一个IL-1α敲低的MLL-AF9 AML细胞系(shIL-1α AML),并注射到WT小鼠中进行DNR治疗,研究发现shIL-1α组的IL-1α水平明显低于对照组(图5K-N)。综上所述,DNR治疗诱导了AML小鼠的肿瘤坏死,从而受损的肿瘤细胞产生IL-1α被释放到血液中,并在化疗期间进一步干扰心功能。
6. IL-1α/NF-κB通过下调PGC-1α来干扰心脏代谢
为了进一步探究DNR治疗后血浆中IL-1α水平的升高干扰心脏能量代谢的机制。研究发现过氧化物酶体增殖物激活受体(PPARs)信号传导通路被显著抑制(图6A),核因子κB(NF-κB)信号通路与PPARGC1A(PGC-1α)之间存在密切联系(图6B)。基于上述结论推测IL-1α/NF-κB可以通过抑制AML+DNR小鼠的PGC-1α信号通路来减弱心脏脂肪酸代谢和线粒体功能。还发现AML+DNR小鼠的PGC-1α表达水平显著降低,p-p65水平显著升高(图6C和D)。那么在IL-1α治疗后,心肌细胞中的IL-1α/NF-κB/PGC-1α通路是否会被激活?在IL-1α处理后,H7-CMs中的NF-κB蛋白水平显著降低,且呈剂量依赖性。同样,PGC-1α表达显著下降,而这些下降被p65敲低所逆转(图6E-G)。总而言之,IL-1α可以通过p65通路抑制PGC-1α的表达。
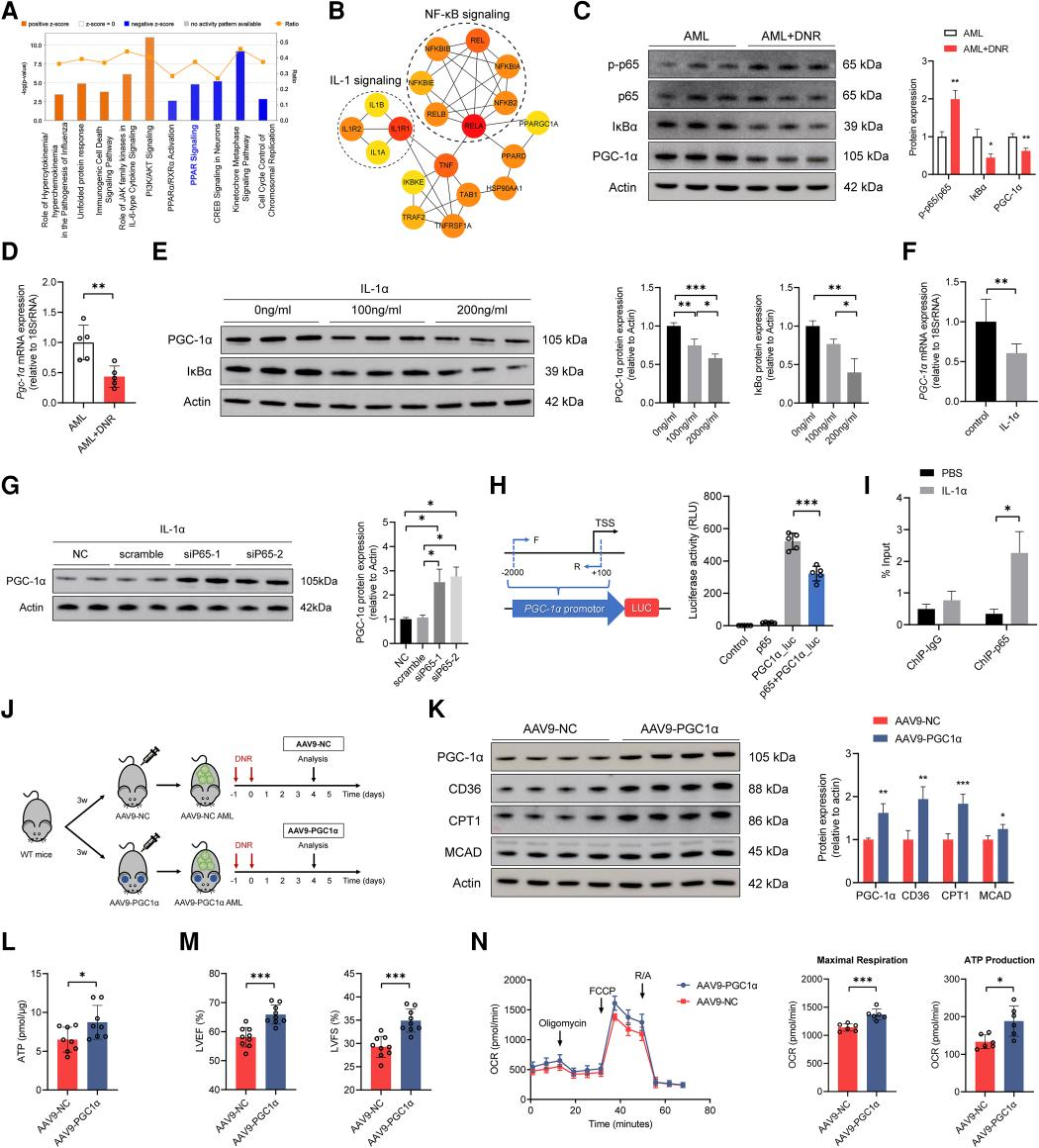
图6. IL-1α/NF-κB通过抑制PGC-1α来干扰心脏代谢
p65是否在转录水平上调控PGC-1α的表达?研究发现由PGC-1α启动子驱动的荧光素酶活性显著降低(图6H)。p65可以与H7-CMs中的PGC-1α启动子发生结合(图6I)。另外研究还发现心脏过表达PGC-1α显著改善了化疗后AML小鼠的心肌ATP浓度和心功能(图6J-N)。综上所述,DNR治疗后,肿瘤细胞释放的IL-1α激活心脏NF-κB信号通路,进一步抑制PGC-1α的表达,导致心脏代谢紊乱和心功能下降。
7. IL-1α中和抗体可以减少DNR化疗后AML小鼠的心脏毒性
该研究提出IL-1α抗体是否可以改善其心脏功能。AML+DNR小鼠用IL-1α抗体或免疫球蛋白G(IgG)处理(图7A和B),之后的数据表明IL-1α抗体治疗组的心脏表现较好(图7C和D)。在心脏代谢方面,IL-1α抗体治疗挽救了代谢重编程,恢复了心肌ATP水平和线粒体功能(图7E-G)。重要的是,IL-1α抗体处理组的心肌PGC-1α和脂肪酸代谢相关蛋白的表达也明显高于对照组(图7H-J)。综上所述,这些结果提示IL-1α抗体可以在不影响DNR化疗的疗效下缓解DNR化疗后导致的心脏底物重构,并能改善心脏功能。
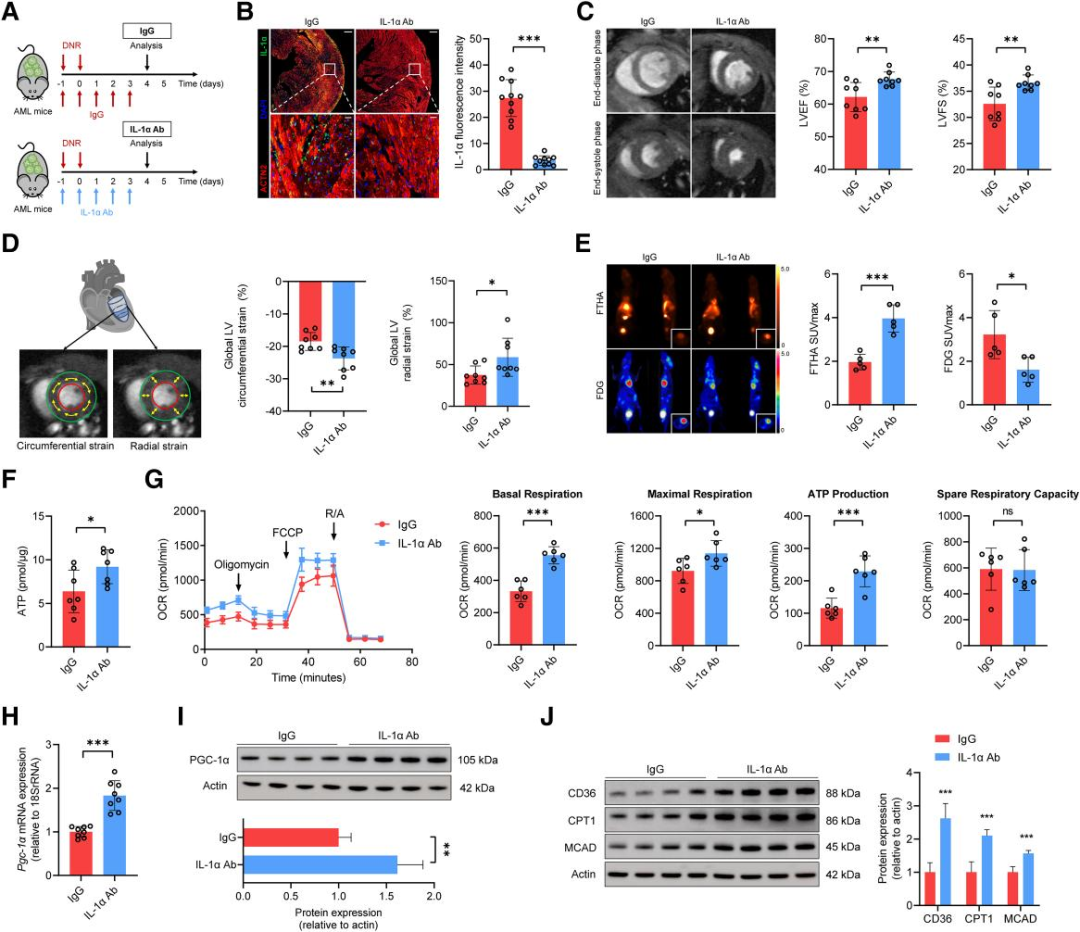
图7. IL-1α中和抗体可以缓解DNR诱导的心脏毒性
研究结论
化疗后肿瘤的变化可能比化疗药物本身对心脏影响更重要的。这篇研究基于DNR化疗后患者标本中心肌细胞代谢状态的改变和动物实验中的多次探索和研究。结果发现肿瘤来源的IL-1α是导致DNR治疗后AML小鼠心脏代谢紊乱和心脏功能受损的原因。其过程是DNR化疗后导致的坏死肿瘤细胞释放IL-1α到血液中,之后与心脏中的IL1R1结合导致NF-κB信号通路的激活,此时会抑制了心肌表达PGC-1α,进而干扰了脂肪酸的利用,并导致心功能的受损(图形摘要)。因此,研究提出IL-1α抗体治疗可以挽救DNR化疗引起的心脏代谢异常,为缓解AML化疗引起的心功能障碍提供了一种新的策略。






