上海百趣生物科技有限公司
13 年
手机商铺
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 2.7
- 2.7
推荐产品
公司新闻/正文
Cell子刊 | 浙大一院黄河团队重大发现:抑制IDH2解锁CAR-T细胞代谢密码,开启抗癌新征程
425 人阅读发布时间:2025-03-31 16:24

英文标题:Mitochondrial isocitrate dehydrogenase impedes CAR T cell function by restraining antioxidant metabolism and histone acetylation
发表期刊:Cell Metabolism
影响因子:27.7
作者单位:浙江大学医学院第一附属医院
百趣提供服务:中心碳代谢
研究背景
嵌合抗原受体(Chimeric Antigen Receptor, CAR)T细胞治疗的疗效受到血液系统恶性肿瘤的复发和实体肿瘤的低反应性的阻碍。长期记忆CAR-T细胞对于提高肿瘤清除和实现长期保护至关重要。然而,在体外快速扩增或体内肿瘤根除过程中,代谢转移和信号抑制导致CAR-T细胞的最终分化和衰竭。在本研究中,作者对CAR-T细胞进行了靶向线粒体化合物药物的筛选以及采用中心碳代谢、单细胞测序等系列研究,发现FDA批准的异柠檬酸脱氢酶2(Isocitrate Dehydrogenase 2, IDH2)抑制剂ENA(enasidenib)可增强记忆CAR-T细胞形成,并在体内维持抗白血病细胞毒性;IDH2通过磷酸戊糖途径抑制葡萄糖的利用,特别是在营养限制的条件下,减少氧化应激,阻碍CAR-T细胞的代谢适应性,同时限制细胞内乙酰辅酶a水平,阻止促进记忆细胞形成的组蛋白发生乙酰化。因此,结合IDH2抑制药物,CAR-T细胞疗法在临床前模型中有望更具优越疗效。
研究概览
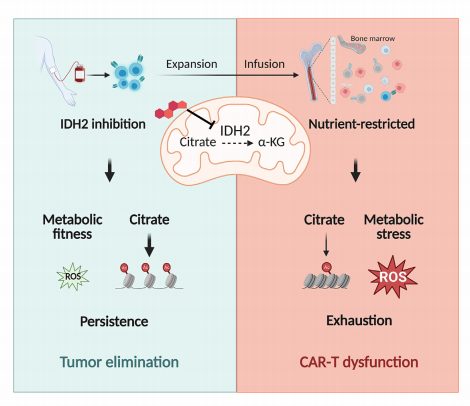
研究成果
1.线粒体相关靶向药物筛选确定ENA,可增加记忆CAR-T细胞形成
为了鉴定影响CAR-T细胞长期疗效的线粒体相关的靶向化学药物,作者对157种线粒体靶向药物进行了体外筛选。在第一轮筛选中,发现37种化合物可以提高CAR-T细胞扩增或CD19+B细胞急性淋巴细胞白血病(B-ALL)细胞(Nalm6)刺激条件下CAR-T细胞的活力。
为了评估药物通过靶向线粒体增强CAR-T细胞治疗持久性的效力,基于CD62L+CAR-T细胞亚群(主要包含T记忆干细胞(Tscm)和中央记忆T细胞(Tcm)的富集),作者对37种化合物进行了第二轮筛选。在促进记忆CAR-T细胞形成的候选化合物中,ENA(AG-221)是最有效的,它是野生型和突变型IDH2酶的抑制剂(图1)。作者通过单细胞转录组等实验进一步验证了ENA处理导致了记忆T细胞亚群的富集和CAR-T细胞中耗竭的T细胞群的减少。此外,ENA处理后TCF1和BCL2等蛋白的增加证实了持续性和活力的增强。这些结果表明,ENA可以维持体外扩增的CAR-T细胞的记忆表型和低耗竭水平,意味着抗肿瘤能力的增强。
作者通过测量ENA治疗后细胞因子的产生和细胞毒性来评估其效应的功能。在正常条件下ENA处理和相对较高的效靶比(E:T)共培养后,颗粒酶B和IFNγ(干扰素γ)的产生没有增强,但在极低的E:T比为1:10的肿瘤再攻毒实验中,ENA处理的CAR-T细胞表现出增强和持续的细胞毒性。更重要的是,ENA处理的CD62L+记忆富集亚群,而不是CD62L-CAR-T细胞,表现出增强的抗原驱动扩张。
以上这些发现表明,在体外扩增过程中,ENA预处理增进了长寿记忆CAR-T细胞的产生,这些细胞具有更好的抗肿瘤耐久性和改善了衰竭,这与具有不同共刺激结构域和单链可变片段的CAR结构无关。
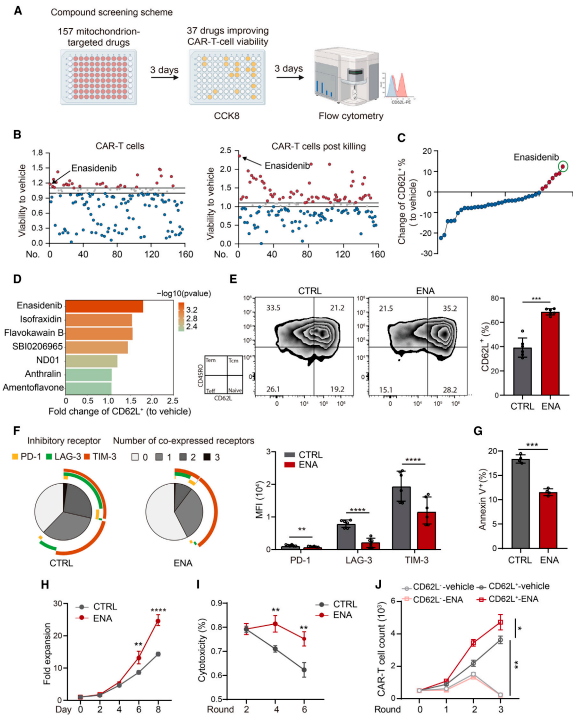
图1 线粒体相关药物筛选识别ENA,可增加记忆CAR-T细胞的形成
2.体内实验证实ENA增强了CAR-T细胞抗肿瘤功能
为了探究ENA治疗对CAR-T细胞介导的抗肿瘤作用,将含有人B-ALL细胞(Nalm6,成熟的白血病细胞)受体小鼠和暴露于ENA或DMSO的CAR-T细胞进行融合。结果显示,ENA预处理的CAR-T细胞比载体预处理的细胞更快地减少肿瘤负担,提供更长的缓解期。在ENA存在的情况下,CAR-T细胞扩增显著延长了输注后受者的存活时间(图2)。通过在早期测量体内CAR-T细胞的存在和白血病负担,发现ENA预处理增强了CAR-T细胞的扩增,使外周血中CD8+细胞的百分比更高。
为了以相对较低的CAR-T细胞输注量延长ENA在难治/复发白血病治疗中的治疗应用,作者通过口服灌胃的方式进行ENA给药。与预期的一样,ENA进一步延长了CAR-T细胞治疗介导的肿瘤抑制时间,增强了CAR-T细胞在骨髓中的持久性,并延长了小鼠的生存期。此外,未经预处理接受CAR-T细胞的患者口服ENA的保护作用低于ENA预处理组,这表明靶抗原和其他环境因子的存在可能会影响ENA增强CAR-T细胞功能的作用。总之,延长体内ENA治疗进一步增强了CAR-T细胞的扩张和肿瘤抑制(图2)。
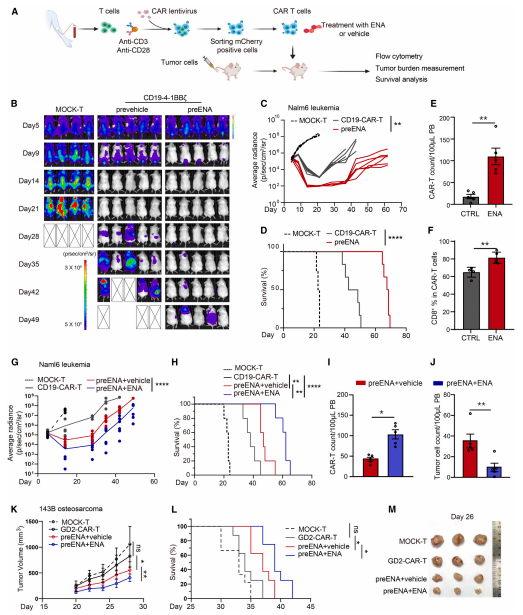
图2 体内实验表明ENA增强了CAR-T细胞的抗肿瘤功能
3.ENA通过抑制IDH2而增强CAR-T细胞的功能
为了探究ENA对CAR-T细胞中IDH酶活性的抑制作用,作者采用以NADP+或NAD+作为辅助因子的线粒体或胞质腔室。结果表明,与IDH1和IDH3相比,ENA主要抑制IDH2的活性(图3),同时ENA处理也明显降低了IDH3活性。作者通过特异性shRNA来敲低IDH2和IDH3A的表达去探究IDH2和IDH3在CAR-T细胞中的作用。结果表明,与ENA治疗的效果一致,IDH2敲低增加了Tscm和Tcm亚群的比例,改善了耗竭,并提高了CAR-T细胞的活力,而不影响CAR转导效率、表达水平和CD8+T细胞的百分比。与ENA一样,IDH2敲低使CAR-T细胞在体外杀死B-ALL细胞后具有持续的细胞毒性。与IDH2敲除不同,IDH3A敲除未引起关于记忆分化和耗竭的任何表型变化。因此,ENA增强的CAR-T细胞功能是对IDH2活性的抑制特异性引起的(图3)。
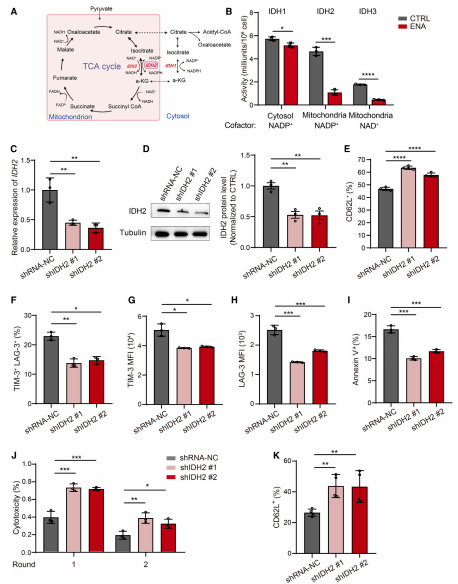
图3 IDH2敲低增强了CAR-T细胞的记忆形成和抗肿瘤功能
4.IDH2抑制实现CAR-T细胞的中心碳代谢重编程
为了评估IDH2抑制是否会改变CAR-T细胞的代谢状态,作者通过测量耗氧量(OCR)来评估线粒体氧化磷酸化(OXPHOS)的活性。结果表明,IDH2抑制对糖酵解活性的降低程度大于对线粒体适应性的影响。此外,作者通过中心碳代谢组学(由上海百趣提供服务)去探究IDH2抑制对CAR-T细胞代谢的影响,中心碳代谢组学结果显示,IDH2抑制增加了葡萄糖6-磷酸(G6P,葡萄糖代谢的第一中间产物)的数量,并上调了CAR-T细胞内己糖激酶的表达(图4)。此外,IDH2抑制后,核糖5-磷酸(R5P)水平和戊糖磷酸途径(PPP)限速酶G6P脱氢酶(G6PD)的表达增加(图4),以及糖酵解代谢产物也发生改变、糖酵解基因表达减少、LDH活性和NADH氧化降低,表明葡萄糖碳利用从糖酵解分流到PPP。这些数据表明,在CAR-T细胞中,IDH2的抑制将葡萄糖碳利用从糖酵解定向到PPP。
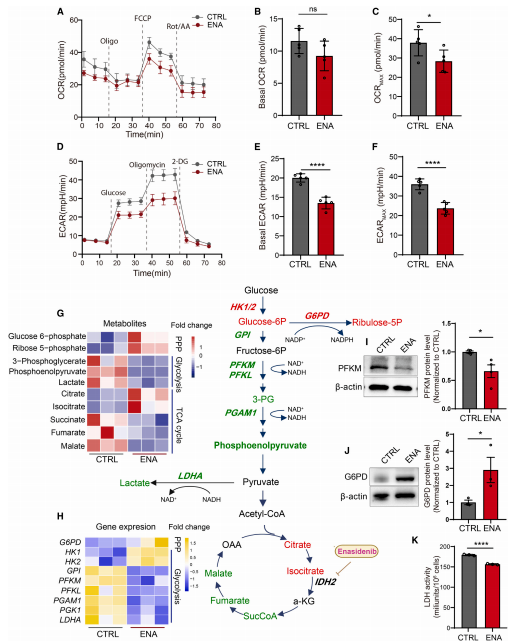
图4 IDH2抑制重组CAR-T细胞的中心碳代谢
5.IDH2消融术诱导活性氧(ROS)水平降低,激活CAR-T细胞
作者使用ROS诱导剂甲萘醌(MENA)、G6PDi-1(一种强效的G6PD抑制剂)等去探究和验证IDH2抑制后CAR-T细胞记忆样表型富集和低耗竭水平的原因以及戊糖磷酸途径(PPP)活性在ENA介导的CAR-T细胞功能增强中的作用。结果显示,IDH2主要通过抑制PPP促进耗竭来阻碍CAR-T细胞的功能,并可能通过其他机制调节CAR-T细胞的记忆形成(图5)。
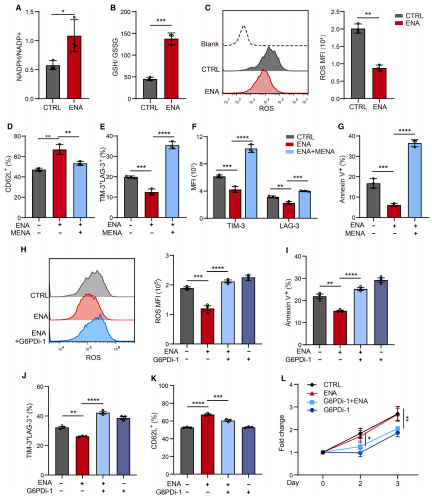
图5 IDH2抑制通过减少活性氧(ROS)来重新激活CAR-T细胞
6.IDH2通过表观遗传调控限制细胞质柠檬酸水平,阻碍记忆CAR-T细胞的形成
作者通过测定细胞质和线粒体的α-KG水平及线粒体和细胞质中分区的柠檬酸盐水平等实验发现ENA治疗后线粒体α-KG水平显著降低,这也表明CAR-T细胞中ENA治疗后IDH介导的氧化脱羧被抑制;且细胞内柠檬酸水平的增加是由细胞质内的对应物引起(图6)。柠檬酸盐能够在细胞质和细胞核之间自由穿梭,并被atp柠檬酸裂合酶(ACLY)分解为乙酰辅酶A,而乙酰辅酶A是通过组蛋白乙酰化实现代谢协调的转录调节的关键介质。为了进一步验证来自柠檬酸的乙酰辅酶A在CAR-T细胞中的作用,作者进行了ACLY抑制和醋酸盐补充。结果发现,ACLY抑制逆转了ENA富集的记忆亚群(图6),而补充醋酸盐促进了CAR-T细胞中记忆亚群的形成。为了确定IDH2抑制后染色质的H3K27ac修饰增加,作者使用抗H3K27ac抗体进行了CUT&Tag测序。结果发现峰值信号在启动子区域显著富集。整合分析CUT&Tag数据和转录组谱,作者确定IDH2抑制后受H3K27ac调控的基因。进一步分析发现,核受体辅抑制因子1 (NCOR1)的H3K27ac水平增强,并且在IDH2抑制后转录增加(图6)。NCoR1可与关键糖酵解基因(如PKM、PFKP和LDHA)的位点结合,并抑制它们在免疫细胞中的表达,这可能是ENA处理的CAR-T细胞中糖酵解减少的原因。总的来说,IDH2抑制增加了CAR-T细胞中特定染色质位点的H3K27ac修饰,导致转录重塑,从而促进记忆T细胞的形成。
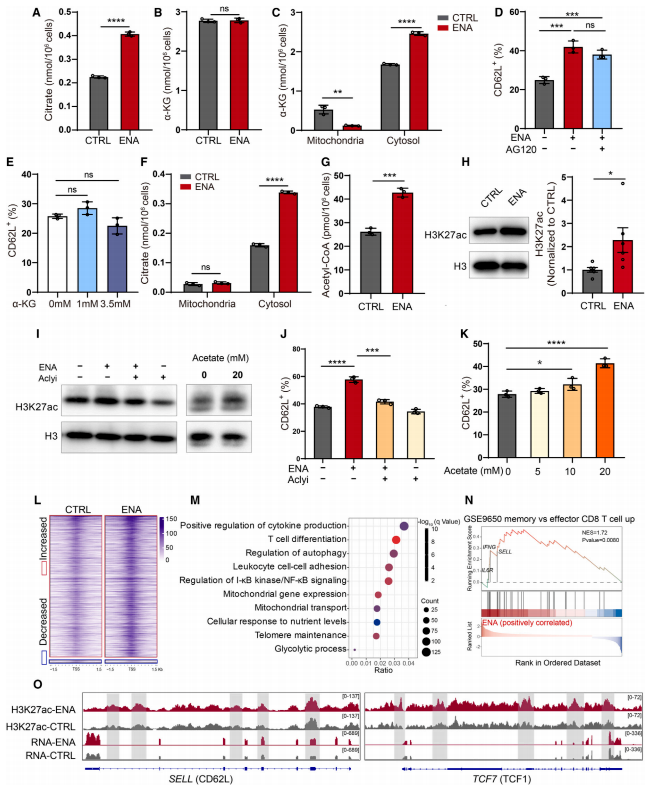
图6 IDH2通过表观遗传调控限制细胞质柠檬酸水平,阻碍记忆CAR-T细胞的形成
7.营养限制通过IDH2介导的葡萄糖散度损害CAR-T细胞的功能
由于CAR-T细胞在极低糖条件下(<1 mM)大量死亡,因此作者在2.5 mM葡萄糖条件下评估了IDH2抑制的效果,并且ENA治疗导致了显著的ROS中和、记忆CAR-T细胞形成和生存优势。为了评估在葡萄糖限制条件下IDH2抑制对CAR-T细胞持久性的影响,作者进行了低E:T比值的连续杀伤试验。即使在第二轮肿瘤攻击期间,ENA预处理也增强了CAR-T细胞功能(图7)。这些结果表明,营养物质有限的恶劣代谢环境会损害CAR-T细胞的功效,而药物抑制IDH2可以通过增强代谢适应性显著增强CAR-T细胞的功能。
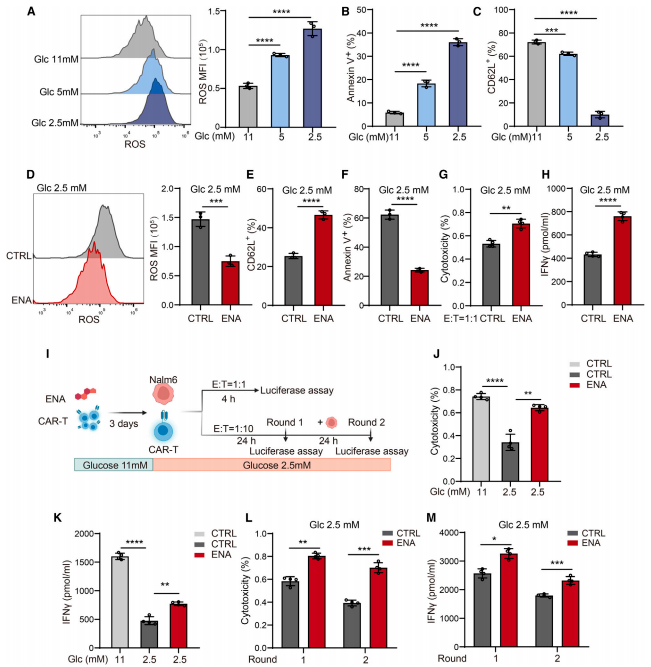
图7 营养限制通过IDH2介导的葡萄糖分歧损害CAR-T细胞的功能
研究总结
本研究通过靶向CAR-T细胞线粒体相关化合物药物的筛选,结果发现FDA批准的IDH2抑制剂ENA可增强记忆CAR-T细胞的形成,并在体内维持抗白血病细胞毒性。由于在体外CAR-T细胞制备过程中有机会进行精确的代谢调节,因此使用药理学方法或基因修饰工具(如crispr)重新连接代谢通路更为可行。通过对健康供体来源的CAR-T细胞进行功能和机制研究,证明了IDH2抑制联合CAR-T细胞治疗在白血病和实体瘤模型中的令人鼓舞的治疗效果,通过药理学抑制IDH2来增强CAR-T细胞的代谢适应性是一种很有前途的策略。






