上海百趣生物科技有限公司
13 年
手机商铺
- NaN
- 0.7000000000000002
- 0.7000000000000002
- 2.7
- 2.7
推荐产品
公司新闻/正文
IF=18.9!浙大医学院副院长吕志民、许大千教授团队揭示调控脂解与线粒体β-氧化的代谢枢纽-糖酵解酶PFKL的神奇作用
171 人阅读发布时间:2025-04-11 16:31

英文标题:Glycolytic enzyme PFKL governs lipolysis by promoting lipid droplet-mitochondria tethering to enhance β-oxidation and tumor cell proliferation
发表期刊:Nature Metabolism
影响因子:18.9
研究背景
肿瘤细胞如何在能量压力下维持生存和增殖的机制?具体来说,研究者们关注了在快速增殖的肿瘤细胞中,特别是在葡萄糖缺乏的情况下,脂滴(lipid droplets)如何通过与线粒体的结合来促进脂肪酸的氧化(β-oxidation),以应对能量压力。文章指出,脂滴与线粒体的结合对于脂肪酸氧化至关重要,但其背后的分子机制尚不清楚。
研究团队发现,糖酵解酶PFKL(磷酸果糖激酶肝型)在葡萄糖缺乏时被磷酸化,降低其活性并促进它与脂滴上的蛋白PLIN2(Perilipin 2)相互作用。PFKL在脂滴上作为蛋白激酶,通过磷酸化PLIN2来促进PLIN2与CPT1A(肉碱棕榈酰基转移酶1A)的结合,进而导致脂滴与线粒体的结合,招募脂肪甘油三酯脂肪酶至结合区域,启动脂质动员。这一过程对于肿瘤细胞的增殖至关重要,干扰这一级联反应可以抑制肿瘤细胞的增殖,促进细胞凋亡,并在小鼠中减缓肝脏肿瘤的生长。本项结果表明,能量压力赋予PFKL另一功能,作为一种蛋白激酶,将脂滴与线粒体连接起来,并突出了PFKL在糖酵解、脂质代谢和线粒体氧化的综合调控中的重要作用。
技术路线
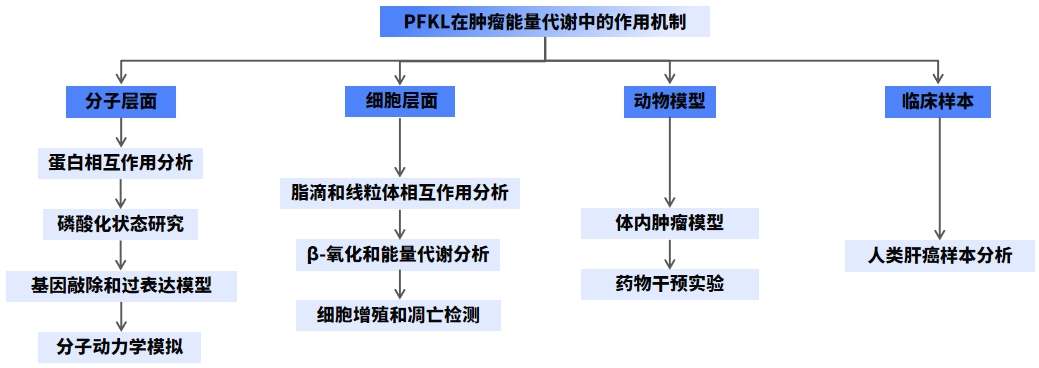
研究结果
1.PFKL是PLIN2和CPT1A之间相互作用、脂滴-线粒体连接和脂滴脂解的必需物质
在能量应激条件下,肿瘤细胞,特别是肝细胞癌(HCC)细胞,依赖脂滴来保持生存和增殖。研究通过LC-MS/MS分析揭示,线粒体外膜蛋白CPT1A与脂滴相互作用,对脂肪酸的β-氧化至关重要。实验发现,在葡萄糖缺乏时,PLIN2与CPT1A结合增强,并且这种结合对于脂滴与线粒体的接近和脂滴的稳定是必要的。此外,PFKL作为PFK的同工酶,也在脂滴上被发现,并在葡萄糖缺乏时与PLIN2的结合增强,对脂滴-线粒体结合和脂解过程至关重要。这些结果突出了PFKL在能量应激下促进脂滴与线粒体结合和脂解的关键作用(图1a~o)。
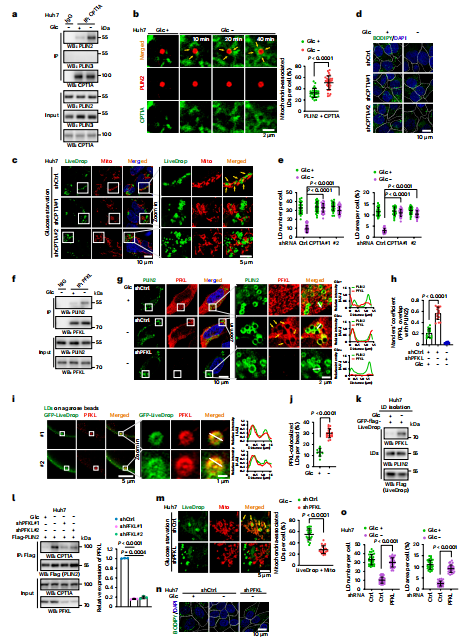
图1 PLIN2和CPT1A之间的相互作用、脂滴-线粒体拴系和脂滴脂解都需要PFKL
2.PFKL作为一种蛋白激酶使PLIN2 Ser159磷酸化
为了解PFKL与PLIN2结合的机制,研究人员在肝细胞癌(HCC)细胞中使用抑制剂阻断信号通路,发现p38 MAPK抑制处理显著减少了葡萄糖缺乏下PFKL与PLIN2的相互作用。研究指出,葡萄糖缺乏促进p38与PFKL结合,并在Thr331位点磷酸化PFKL,这一位点在物种间保守。通过同源建模和分子动力学模拟,研究人员发现Thr331磷酸化可能影响PFKL四聚体稳定性,导致其向单体转化,影响PFKL的糖酵解活性。此外,PFKL作为蛋白激酶,能磷酸化PLIN2的Ser159位点,这一过程不依赖其代谢活性,而是通过改变催化结构域实现,对肿瘤细胞生存和增殖至关重要(图2a~m)。
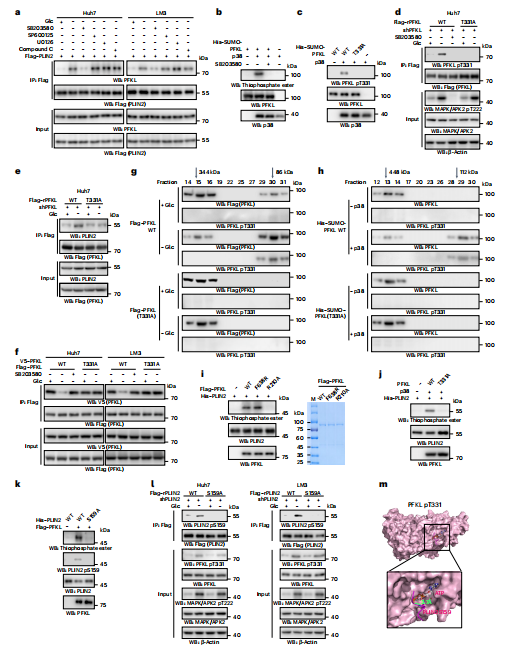
图2 PFKL作为蛋白激酶,使PLIN2 Ser159磷酸化
3.PFKL介导的PLIN2Ser159磷酸化促进PLIN2与CPT1a的相互作用、脂滴-线粒体拴系和β氧化
研究人员探究了PLIN2蛋白在Ser159位点的磷酸化对其与CPT1A形成复合物、脂滴与线粒体结合以及脂肪酸β-氧化的影响。使用谷氨酰胺剥夺的Huh7和LM3细胞,发现只有PFKL磷酸化的野生型PLIN2能与CPT1A结合,而Ser159位点突变为丙氨酸(S159A)的PLIN2则不能。Ser159磷酸化促进了脂滴与线粒体的结合和BODIPY-C12的转运,而S159A突变体阻断了这些过程。此外,Ser159磷酸化减少了PLIN2与ATGL的结合,可能通过结构变化暴露脂滴膜,促进ATGL的脂解作用。ATGL耗竭显著抑制了脂滴消失,显示其在脂滴消耗中的关键作用。Seahorse FAO实验显示,葡萄糖剥夺或2-DG处理增加β-氧化率,这可被rPLIN2(S159A)、 rPFKL(T331A)或etomoxir阻断,表明PFKL介导的PLIN2 Ser159磷酸化促进了HCC细胞在能量应激下的β-氧化(图3a~l)。
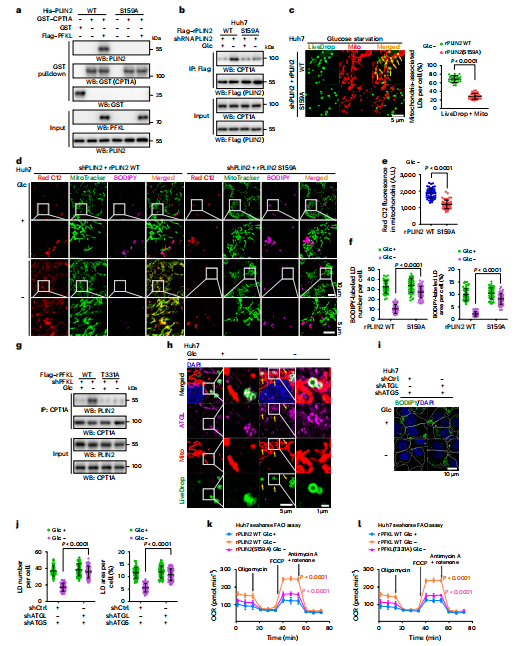
图3 PFKL介导的PLIN2Ser159磷酸化促进PLIN2与CPT1a之间的相互作用、脂滴-线粒体拴系和β氧化
4.PFKL介导的PLIN2 Ser159磷酸化促进肝癌细胞存活、增殖和肿瘤生长
癌细胞通过β-氧化来抵消能量压力,以维持生存和细胞增殖。葡萄糖缺乏会提升Huh7肝癌细胞的凋亡,2-DG处理降低癌细胞的增殖。使用etomoxir或表达特定突变体rPLIN2(S159A)和rPFKL(T331A)会加重葡萄糖缺乏对细胞的影响,但补充短链和中链脂肪酸能显著恢复由此增加的细胞死亡,表明PFKL介导的PLIN2 Ser159磷酸化有助于细胞在葡萄糖缺乏下生存。研究人员进一步通过在裸鼠体内注射表达野生型和突变体rPLIN2与rPFKL的Huh7细胞,发现这些突变体表达抑制了肿瘤生长,减少了肿瘤体积和重量,并伴随脂滴积累增加、细胞死亡增强和Ki67表达降低,揭示了PFKL在肿瘤生长中的重要角色。2-DG处理通过抑制糖酵解减少脂滴数量,抑制肿瘤生长,并增加PLIN2 Ser159和PFKL Thr331的磷酸化。rPLIN2(S159A)或rPFKL(T331A)与2-DG联合处理进一步抑制肿瘤生长,减少脂质消耗和Ki67表达。这些结果表明PFKL介导的PLIN2 Ser159磷酸化促进了肝细胞癌细胞的生存、增殖和肿瘤生长(图4a~h)。
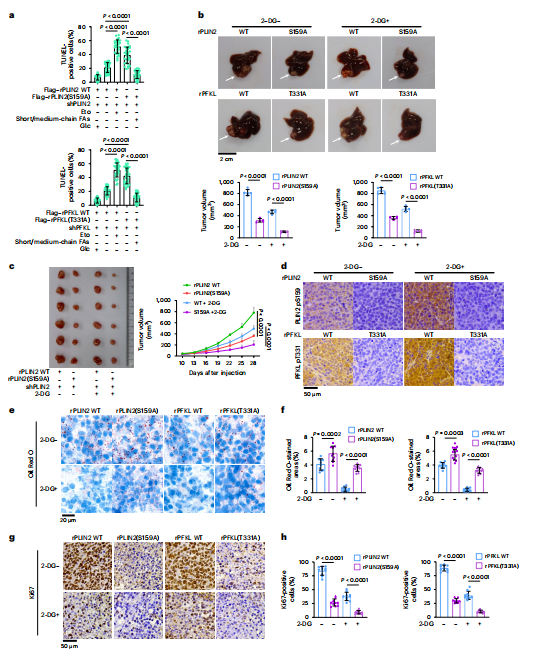
图4 PFKL介导的PLIN2 Ser159磷酸化促进肝癌细胞的存活、增殖和肿瘤生长
5.PFKL介导的PLIN2 Ser159磷酸化与人肝癌的临床侵袭性相关
研究人员通过免疫组化染色分析人类肝细胞癌(HCC)及正常组织样本,发现HCC样本中PFKL的Thr331和PLIN2的Ser159磷酸化水平显著高于正常组织,且这两个位点的磷酸化在HCC中正相关。定量分析确认了这些相关性,并通过癌症蛋白基因组数据分析网站的数据集发现了PLIN2 Ser159位点磷酸化的上调。PFKL Thr331和PLIN2 Ser159的磷酸化水平与HCC患者生存率差相关联,表明p38介导的PFKL及其介导的PLIN2磷酸化在HCC的临床侵袭性中扮演关键角色(图5a~e)。
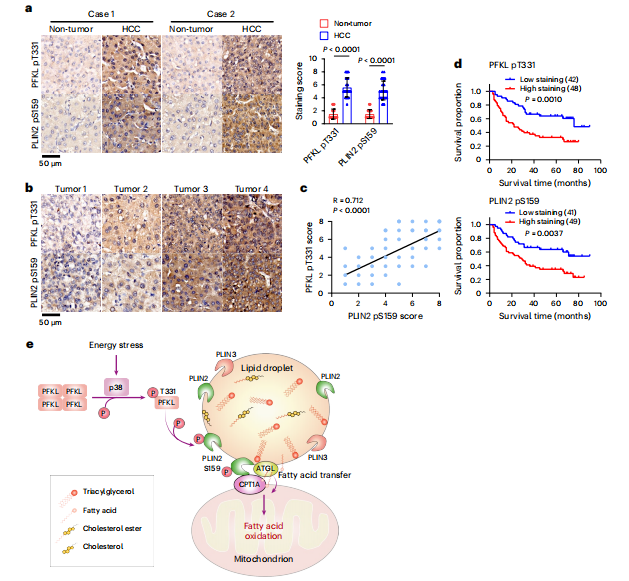
图5 PFKL介导的PLIN2 Ser159磷酸化与人肝细胞癌的临床侵袭性相关
结论
在葡萄糖缺乏时,脂滴蛋白PLIN2与线粒体蛋白CPT1A结合,CPT1A耗竭会阻断脂滴与线粒体结合并减少脂滴数量。研究显示,葡萄糖缺乏激活p38,磷酸化PFKL的Thr331位点,导致其从四聚体变为单体,抑制其代谢活性。磷酸化的PFKL与PLIN2结合,磷酸化PLIN2的Ser159位点,促进脂滴与线粒体结合,招募ATGL,促进脂肪酸转移和β-氧化。PFKL和PLIN2的磷酸化位点突变可抑制肿瘤细胞增殖,促进凋亡,减缓小鼠肝脏肿瘤生长。这揭示了PFKL在低糖酵解条件下的新功能,即促进脂滴与线粒体结合,促进脂肪酸转移和β-氧化。PFKL作为糖酵解酶,也具有耦合脂质和线粒体代谢的蛋白激酶功能,其在HCC细胞中的作用与患者生存率相关,表明其在癌症治疗中的潜在靶点价值。






